Маски для быстрого роста волос
24 июля 2023 680 0Длинные, густые и шелковистые волосы всегда были и есть эталоном женской красоты. О них писали в стихах и слагали легенды. Если ваша мечта иметь роскошные волосы,...
Читать далее »Как увеличить глаза с помощью макияжа
20 июля 2023 765 0Макияж – это создание гармоничного лица, в котором акцент делается на глаза либо на губы. Выделение того и другого в дневном make up считается вульгарным и...
Читать далее »Свои секреты красоты
18 ноября 2022 836 0Краски для волос аллергику Перед окрашиванием бровей и ресниц вам следует знать о некоторых вещах. Проводить окраску можно только в том случае, если нет...
Читать далее »Ребёнку психологически комфортно
17 ноября 2022 7063 0Ребёнка вновь интересует грудь мамы Довольно сложная ситуация. Общение ребёнка с грудью матери всегда зеркально показывает взаимопонимание ребёнка и...
Читать далее »Маму волнуют вопросы
16 ноября 2022 1053 0Почему ребёнок плачет? Плач — своеобразный язык младенцев. Таким образом малыш подаёт нам сигнал о том, что ему, что — то не нравится, он чем — то обеспокоен....
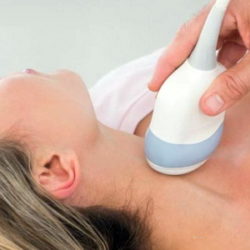
Читать далее »Влияние щитовидной железы и эрозии на роды
14 ноября 2022 544 0Проблемы со щитовидной железой влияют на репродуктивную функцию Заболевания щитовидной железы относятся к экстрагенитальной патологии, которая может...
Читать далее »Секреты красоты лица
13 ноября 2022 665 0О лазерной чистке лица Лазерная чистка лица проводится при воздействии лазерного луча на проблемные зоны кожи. При таком воздействии ороговевшие клетки...
Читать далее »Лечение эндометриоза
12 ноября 2022 646 0Эндометриоз Эндометриоз — это состояние, когда по причине травмы, заброса менструальной крови через трубы в брюшную полость, кесарева сечения и т. п.,...
Читать далее »Агрессивное поведение детей
11 ноября 2022 699 0Борьба малыша за свои права Под агрессией понимается активность детей, и в ней нет ничего плохого. Ваш сын борется за своё право обладать жизненными благами. В...
Читать далее »С удовольствием кормить малыша грудью
10 ноября 2022 670 0Обстановка при кормлении Во время кормления очень важно уделять ребенку всё ваше внимание (особенно первые 20 минут) — смотреть ему в глазки, делать массажик...
Читать далее »- Готовимся к лету: диеты
- Диеты (видео)
- Женская диета
- Женская красота
- Женская мода
- Женская психология (видео)
- Женские рецепты
- Интимные отношения (видео)
- Красота женщины: уход за собой
- Лучшие книги для женщин
- Любящая мама
- Мода и красота (видео)
- Поздравление женщине
- Психология женщин в отношениях
- Психология женщины
- Разное — полезное
- Самые успешные женщины
- Сохраним здоровье